サンフランシスコ--(BUSINESS WIRE)--(ビジネスワイヤ) -- 49施設からのAMI心原性ショック(AMICS)継続患者250人に関する全国心原性ショック・イニシアチブ研究(NCSI)の本日発表されたデータは、72%の生存退院率と98%の自己心機能回復率を示しています。患者はNCSIプロトコルによる治療を受けましたが、同プロトコルは経皮的冠動脈インターベンション(PCI)を通じた血行再建に先立ち、アビオメッド(NASDAQ: ABMD)のImpella心臓ポンプを留置するものです。研究では、心原性ショックにおける生存率を本プロトコルで向上させるアプローチが、米国の学術病院や地域病院で再現可能であることが示されました。研究結果は、サンフランシスコで開催中の第31回経カテーテル心血管治療学(TCT)会議にて、ヘンリー・フォード病院の構造的心疾患センターでメディカルディレクターを務めるウィリアム・オニール医師(MD)が発表しました。
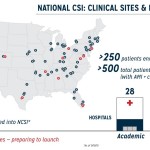

NCSIの実施以前、心原性ショックの生存率はここ20年の間、約50%にとどまっていました。医師主導型のNCSIの研究者らは、プロトコルを実践することで生存率を向上させ、自己心の回復を達成しています。
NCSIのプロトコルの元になるベストプラクティスには、心原性ショックの早期発見、循環作動薬の使用の最小化、血行再建(PCI)に先立つImpella CP留置が含まれます。PCI前にImpellaを留置するベストプラクティスを支える証拠は、Impella IQデータベース、cVAD研究、Hannover Registry、デトロイト心原性ショック・イニシアチブの何千人という患者から得られたものです。
研究者らは現在、Impella補助下PCI直後のカテーテルラボに適用する新しいエスカレーション・プロトコルを策定して、患者の生存率と自己心回復率をさらに向上させることを計画しています。エスカレーション・プロトコルは、心原性ショック・ワーキング・グループ、cVAD研究、NCSI初期データから得た知見に基づいています。
エスカレーション・プロトコルは具体的に次の内容となります。
Impella補助下PCIの後、患者が1種類の循環作動薬を使用中で心拍出力(CPO)が0.8ワット未満の場合、6時間以内にImpella 5.0にレベルアップする。
Impella補助下PCIの後、患者が右心室機能不全を呈する場合、速やかにImpella RPにレベルアップするか酸素供給を実施する。
ヘンリー・フォード病院の構造的心疾患センターでメディカルディレクターを務めるウィリアム・オニール医師(MD)は、次のように述べています。「追加的な補助が必要な患者を速やかに発見してエスカレートすることで、心原性ショックにおける生存率を75%まで向上させることができると思います。Impella心臓ポンプの早期留置を含む標準化プロトコルの使用により、生存率と自己心回復率を劇的に向上できることは、米国中の医師がすでに証明しています。これらの新しいエスカレーション・プロトコルは、さらに多くの患者が自宅に帰宅することに役立ちます。」
アビオメッドはFDA承認の取得以来、米国のImpella使用患者のほぼ100%に関するデータを、観察的IQデータベースに収集しています。この臨床データは、アビオメッドの前向きcVAD研究に組み込まれたFDA承認後試験とともに、生存率および自己心回復率の改善に伴うImpella使用のベストプラクティスを確認・検証することに役立っています。
アビオメッドの最高医学責任者(CMO)であるSeth Bilazarian(MD)は、次のように述べています。「心原性ショックは末端器官の重篤な低かん流状態をもたらすものであり、Impellaによるアンロードは患者にとってFDA承認の治療法となります。複数のレジストリーや研究で収集された実臨床証拠から導いたプロトコルは、PCIに先立ってのImpellaによるアンロードが生存率改善にとって不可欠な要素であることを示しています。」
Impellaは心原性ショックの治療法としてFDAより最高水準の承認を取得しており、心室の仕事量を減らして心臓の回復と残存心筋機能の早期評価を可能にするために必要な循環補助を提供するものです。
IMPELLA心臓ポンプについて
Impella 2.5®およびImpella CP®の各デバイスは、閉塞した冠動脈を再開通するためにステント留置術またはバルーン血管形成術などの選択的で緊急の経皮的冠動脈インターベンション(PCI)を受ける一定の進行性心不全患者の治療を目的として、米国FDAより市販前承認(PMA)を取得しています。Impella 2.5、Impella CP、SmartAssist®搭載Impella CP、Impella 5.0®、Impella LD®、SmartAssist®搭載Impella 5.5™は、心原性ショックを呈する心臓発作/心筋症患者の治療に使用する心臓ポンプとして米国FDAの承認を取得しており、生来の心臓回復を可能にし、患者が自身の心臓のまま帰宅できるようにする独自の能力を備えています。Impella RP®は、左心補助人工心臓埋め込み、心筋梗塞、心臓移植、心臓切開手術の後の右心不全または代償不全の治療を目的として米FDAの承認を受けています。Impellaは、FDA史上で最も研究された機械的循環補助デバイスで、10万人以上の患者に関する実臨床データ、550本以上の査読付き論文が存在します。
欧州でImpella 2.5、Impella CP、SmartAssist搭載Impella CPは、高リスクPCIおよび急性心筋梗塞(AMI)の心原性ショック患者の5日目までの治療を目的としてCEマークを取得しています。Impella 5.0およびImpella LDは、心原性ショックを呈する心臓発作/心筋症患者の10日目までの治療を目的としてCEマークを取得しています。Smart Assist®搭載Impella 5.5™心臓ポンプは、心原性ショックを呈する心臓発作/心筋症患者の30日目までの治療を目的としてCEマークを取得しています。Impella RPは、左心補助人工心臓埋め込み、心筋梗塞、心臓移植、心臓切開手術、難治性心室性不整脈の後の右心不全または代償不全の治療を目的としてCEマークを取得しています。
承認された適応症や、デバイスの使用に伴う重要な安全性・リスク情報を含め、Impella心臓ポンププラットフォームの詳細については、www.impella.comをご覧ください。
アビオメッドについて
米マサチューセッツ州ダンバースに拠点を置くアビオメッドは、循環補助用の医療機器を提供する一流企業です。当社製品は血流の改善もしくは心臓のポンプ機能の実行または両方により心臓を休止させるよう設計されています。詳細情報については、www.abiomed.comをご覧ください。
Abiomed、Impella、Impella 2.5、Impella 5.0、Impella LD、Impella CP、Impella RP、Impella Connectは、アビオメッドの登録商標で、米国および一定の外国で登録されています。Impella BTR、Impella 5.5、Impella ECP、CVAD Study、SmartAssistはアビオメッドが登録申請中の商標です。
将来見通しに関する記述
本リリースは、アビオメッドの既存製品および新製品の開発、商業的成長に向けた当社の進捗状況、将来の機会および期待される規制関連の承認に関する記述を含め、将来見通しに関する記述を含んでいます。当社の実際の成績は、多くの要因のため、これらの将来見通しに関する記述で予想された内容とは大きく異なる場合があります。それらの要因には、開発、試験、関連する規制上の承認に伴う不確実性(将来の損失の可能性を含む)、複雑な製造、高品質の要件、限られた供給源への依存、競争、技術の変化、政府の規制、訴訟関連の問題、将来の資金需要と追加資金調達の不確実性、最新のフォーム10-K年次報告およびフォーム10-Q四半期報告を含め、当社が米証券取引委員会に提出した書類で詳述したその他のリスクや問題が含まれます。これらの将来見通しに関する記述は、本リリースの日付時点での言及に過ぎず、過度の信頼を寄せないように注意をお願いします。当社は、これらの将来見通しに関する記述に対するいずれの訂正についても、その結果を公表する義務を負いません。これらの訂正は、本リリースの日付以降に発生する出来事や状況を反映させたり、予想外の出来事を反映させたりする場合に行われる可能性があります。
本記者発表文の公式バージョンはオリジナル言語版です。翻訳言語版は、読者の便宜を図る目的で提供されたものであり、法的効力を持ちません。翻訳言語版を資料としてご利用になる際には、法的効力を有する唯一のバージョンであるオリジナル言語版と照らし合わせて頂くようお願い致します。
Contacts
Tom Langford
Director, Communications and Public Relations
978-882-8408
tlangford@abiomed.com
Ingrid Goldberg Ward
Director, Investor Relations
978-646-1590
igoldberg@abiomed.com
